自2020年新冠傳染病爆發以來,生物制藥/生物工藝行業在進行有效的應對過程中,也加劇了供應鏈挑戰、人才短缺和行業區域化等問題,同時產生了新的戰略發展需求。2021年在BioPlan Associates發表的18th Annual Report and Survey of Biopharmaceutical Manufacturing Capacity and Production,通過對包括25個國家的生物工藝行業單位的140名決策者(包括生物藥企和CDMO公司)和100名供應商調查采訪,對生物工藝工業發展的現狀和趨勢進行了討論。
生物工藝行業發展現狀
目前全球行業機構、資本和藥企都在對生物制藥行業生產設施進行大量資源投入,生物工藝產能和生產能力也在不斷提高。但需注意的是,生物藥物的高成本以及政府實施的價格控制,會繼續對該行業構成威脅。
BioPlan的Top 1000 Global Biopharmaceuticals Facilities Index統計追蹤顯示, 目前全球生物工藝產能約為1730萬升 ,包括1625個生物制藥/生物工藝設施,美國562個,中國224個,印度109個,德國83個,法國38個,日本36個,加拿大35個,比利時26個,意大利23個,瑞典22個,俄羅斯21個,巴西20個,丹麥17個,奧地利15個,西班牙12個,馬來西亞10個,阿根廷7個,墨西哥7個,南非7個,泰國6個,愛爾蘭6個,埃及5個,古巴5個。
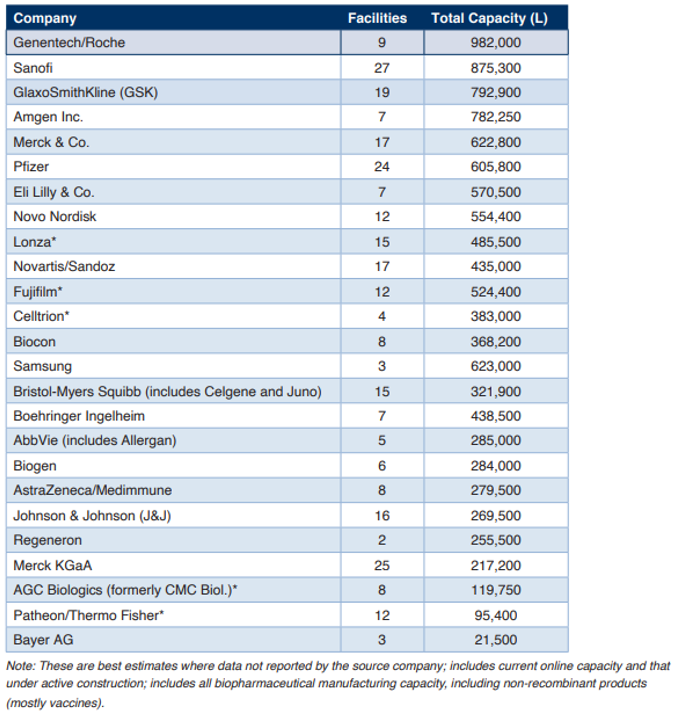
全球大部分生物工藝產能集中在數量相對較小的大型生產基地中,前100個的生產基地產能約占全球占比三分之二。其中區域分析顯示: 美國/北美產能約為549.6萬升(占比31.7%) ,同時擁有最多的CMO,包括涌現大量針對新型療法CGT的CMO。 歐洲產能約為598.3萬升(占比34.7%)。亞洲和其它產能約為582.6萬升(占比33.6%) ,亞洲在數量上正接近美國,但其平均產能仍然較低,并存在高度集中,如韓國Celltrion和Samsung。
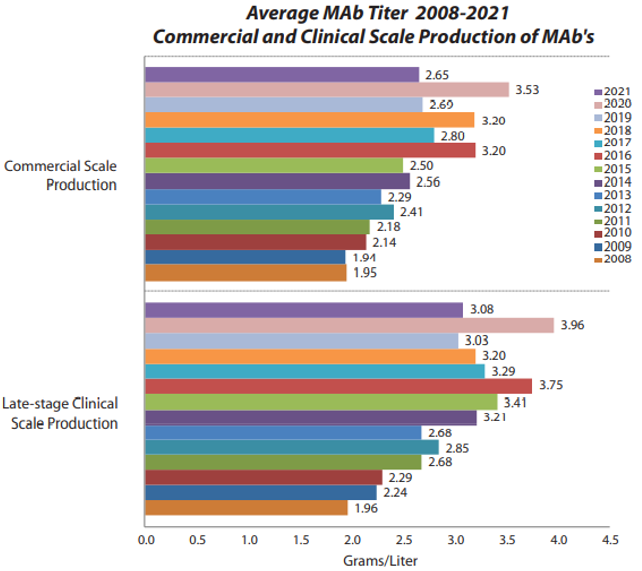
全球生物工藝生產能力也在繼續逐步提高,主要是在于上游表達量的提高,下游純化回收率的提升較小。2008年至2021年,商業化生產規模的平均表達量由1.95g/L提高至2.65g/L,年增長率為2.4%;臨床后期生產規模的平均表達量由1.96g/L提高至3.08g/L,年增長率為3.5%。
生物工藝行業發展趨勢
生物新藥/生物類似藥持續增長
在全球生物制藥行業,美國繼續保持行業領先地位,更加重視創新、研發、工藝開發和臨床生產,擁有最多的生物工藝設施數量,同時亞洲等新興地區也在快速發展。全球目前有越來越多的生物新藥、生物類似藥進入市場,生物制藥產業已進入成熟階段,同時許多新參與者通過生物類似藥進入生物制藥行業,并建設新的生產基地。
FDA生物藥的批準一直在穩步增長,2020年,FDA(包括EUA)批準了29種生物藥,19個是重組單克隆抗體,3個生物類似藥,3個疫苗(非重組),2個酶,1個細胞療法,1個ADC藥物,基因治療獲批為0。
全球約有1100種生物類似藥正在研發或銷售,其中近600種正在臨床試驗中或商業化銷售。CMO行業報告顯示生物類似藥業務增長約15%。生物類似藥主要市場是美國和西歐,有約80種生物類似藥被批準,其中FDA已經批準了29款生物類似藥。
生物工藝加速技術創新
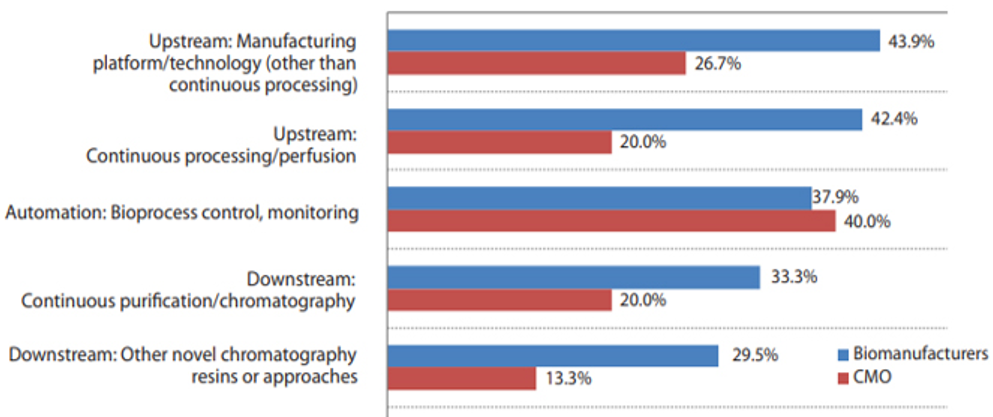
提高效率和生產力等的生物工藝創新方法將在未來幾年獲得更多的認可。當今被問及最需要哪些生物工藝創新時,受訪者大部分集中在連續生物工藝的各個方面。
• 超過 40% 的受訪者表示“上游:制造平臺/技術(連續加工除外”(42.2%)和“上游:連續加工/灌注”(40.1%)將成為明年測試評估的領先生物工藝系統 .
• "自動化:生物過程控制和監測"(占37.9%)也被認為是今年將進行評估的重要領域。
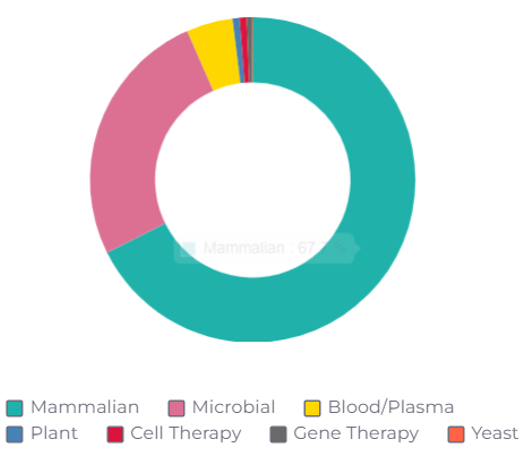
哺乳動物系統繼續占據主導地位
哺乳動物細胞培養繼續占據生物制藥的開發和制造主導地位, 其中中國倉鼠卵巢(CHO)細胞系繼續徹底主導, ,同時擁有最多的CMO,包括涌現大量針對新型療法CGT的CMO。同時其它哺乳動物細胞系也越來越多地被使用,例如,HEK293用于單克隆抗體和其他重組蛋白,現在也用于AAV和其他基因治療病毒載體制造。
一次性系統的接受度逐步提高
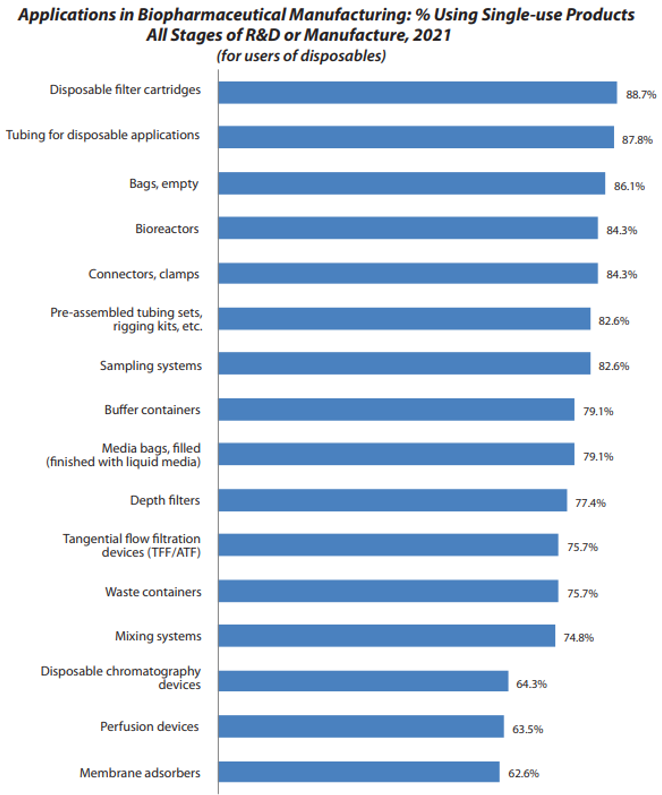
BioPlan預估≥85%的研發和臨床用生物藥物產品是涉及基于一次性系統進行生產制造。在接受調查的20多個SUS地區中,超過80%的受訪者表示目前大量使用一次性生物工藝設備。生物工藝行業的許多趨勢,包括一次性技術,都是由對提高生產率、質量和降低制造過程中成本的持續需求所驅動。
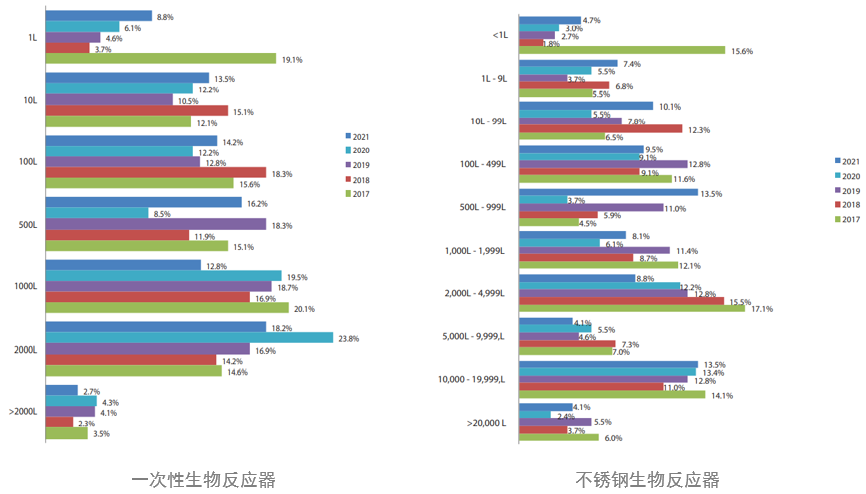
不銹鋼生物反應器規模尺寸更小
隨著一次性生產設施更多的上線,生產工廠中運行的不銹鋼生物反應器體積規模正在逐步下降,尤其是更大規模的不銹鋼生物反應器(≥2000升)。如今一次性生物反應器在研發和早期臨床生產中廣泛使用,其中估計≥85%是使用一次性系統,目前使用一次性生物反應器主流選擇通常是2000升。
但是不銹鋼生物反應器仍然受到許多應用的青睞,特別是在生物藥商業化生產中。選擇由可反復利用的不銹鋼生物反應器生產設施通常更具成本效益。與2019年和2020年(14.8%)相比,2021年有25.0%的受訪者表示現在認為"建設新的不銹鋼設施"是一個非常重要的領域,以避免產能限制,這可能是對大規模、固定生產能力的需求的響應,以應對未來的大流行挑戰。
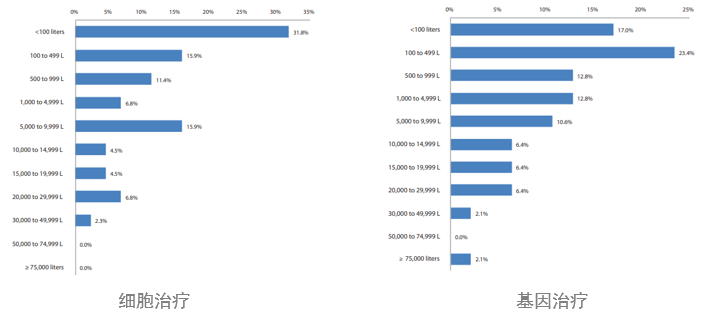
不銹鋼生物反應器規模尺寸更小
在2021年的調查中,對CGT的生產制造設施能力的分析表明,其偏向于較低的生產規模。在涉及細胞療法的調查者中,47.7%的人報告的生物反應器使用總容量低于500L,在涉及基因治療的調查者中,其比例更低為40.0%。受訪者認為基因治療設施的預估需求產能平均為2900升,細胞療法為2700升。%是使用一次性系統,目前使用一次性生物反應器主流選擇通常是2000升。
BioPlan研究還表明,近90%的CGT開發人員更愿意通過CMO進行生產制造,但大多數人沒有在CMO中找到能滿足的所需專業知識、產能和/或設施,或者由于啟動新項目的等待時間較長而不愿意涉入該領域。因此傾向內部自行建立商業生產基地, "內包"趨勢是可能的。BioPlan同時正在密切關注這一趨勢變化。
中國成為生物制藥的主要新參與者
中國生物企業在歐美遞交的臨床IND試驗申請正在加速增長,中國申請美國IND的數量由2010年前的0-2個增長至2018年的33個。
BioPlan最近發布了一份關于中國CMO的報告(Growth of CMOs in China, June 2020)。中國CMO的數量和規模正在快速擴大,其主要原因包括。
• 更多的生物新藥和生物類似藥進入臨床階段;
• 中國生物醫藥的發展和商業化規模生產相對較新,前期會依賴CMO;
• 中國生物藥企數量越來越多,超過100家公司在研發單抗;
• 中國生物工藝總產能超過150萬升,約占全球9.2%(BioPlan報告);
• 中國政府正在修訂醫藥法規,改變以前排除CMO或其它第三方生產生物藥物;
• 龐大的中國人口刺激了生物藥物市場的增長;
• 西方公司對將生物工藝外包給中國的興趣和期望正在增加。
總 結
COVID-19大流行帶來了全球性問題,許多行業在新冠疫情挑戰下發生了重大變化甚至是顛覆性改變。生物制藥/生物工藝行業在應對這些挑戰方面相對有效,它表現出了靈活性,如繼續擴大生物藥物研發和生產設施、線上居家辦公、注重供應鏈安全 (生產基地由以前備貨6-12個月,改為12-18個月) 、優先考慮大流行相關的物料訂單供應和研發投資合作。從長遠來看,生物行業如何處理所吸取的經驗教訓將有助于確保該行業為未來的公共衛生挑戰做好準備。
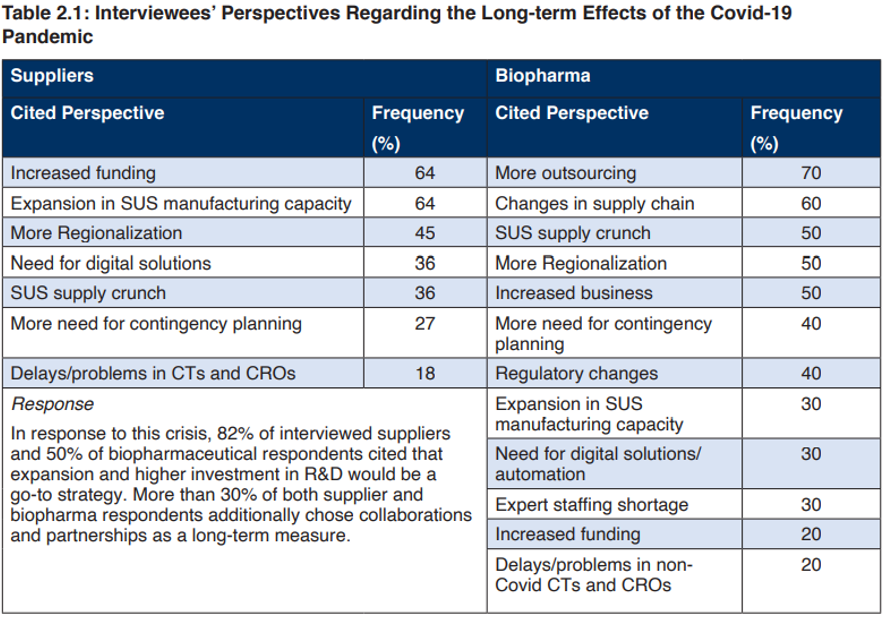
針對COVID-19大流行對生物工藝行業的主要長期影響方面采訪結果顯示,≥50%的受訪者表示長期影響主要集中在 更多的外包、供應鏈的變化、更多的區域化、SUS供應緊縮、當前供應短缺惡化和不確定性 。未來供應鏈安全問題涉及物流、庫存、生產on-shoring、二級供應商等,因此需要主動創建積極供應鏈解決方案應對挑戰,包括避免原材料短缺、物流、跨境庫存和倉儲、以及人員短缺。
備注:
本文內容和圖表主要摘抄于Bioprocessonline和BioPlan Associates,參考資料信息如下:
Langer,E.S., et al.,Report and Survey of Biopharmaceutical Manufacturing Capacity and Production,18th annual edition, BioPlan Associates,Rockville,MD,April 2021,527 pages. Smita Khanna,"2021's Bioprocessing Year In Review & 7 Key Takeaways”BioPlan Associates, January 11, 2022.




























 2022.07.26
2022.07.26
 2022.09.13
2022.09.13
 2022.07.21
2022.07.21